Contaminación ambiental
Cadena contaminada
La contaminación ambiental se le denomina como un factor de riesgo para la salud de todos los seres vivos que habitan en la tierra y se da por los malos hábitos de las propias personas, al arrojar basuras y residuos sólidos en el suelo, en lugar de deposítarlos en una caneca de basura, también existen personas que acumulan la basura en la tierra y luego la queman. La mejor opción para mejorar esta contaminación es aplicar el método de las 3 R, 1 Reducir: Tratar de no malgastar las cosas y hacer residuos innecesarios, 2 Reciclar: Hacer un uso adecuado de los botes de basura, saber que un bote debe depositar el vidrio, en otro el papel, en el siguiente el plástico, en otro el plástico
y en el ultimo lo inorgánico; 3 Reutilizar: Lo que se uso y todavía esta en buen estado nos sirve para hacer una manualidad u otras cosas.
En este vídeo podemos observar la problemática que se vive en la Institución Educativa Cadena las Playas con la contaminación ambiental, es un problema que nos afecta a todos. Todos los estudiantes de esta institución arrojan la basura en el suelo, sabiendo que tienen muy cerca botes de basura, ademas de esto, no son capaz de hacer un aseo bien hecho, dejan basura regada y lo que mas esta afectando es que arrojan la basura en la parte trasera del colegio, la cual se esta deteriorando mucho, no tiene presencia, el techo del restaurante y de la tienda esta muy contaminado con los residuos sólidos, los estudiantes de esta institución deben tener sentido de pertenencia, sabiendo que es un ambiente en donde comparten sus mejores y peores momentos y es su segundo hogar.
Se deberían promover campañas que ayuden a concientizar a todos los estudiantes para que pongan en practica el sentido de pertenencia con su Institución y con ellos mismos, que aprendan a saber usar los botes de basura, reutilizar y reciclar, elaboración de manualidades con materiales ya utilizados en un buen estado; establecer multas a los derrochadores de materiales que se puedan reutilizar y a los que arrojen la basura al suelo nosotras elaboramos un vídeo mostrando toda esta problemática, que se le debe poner un fin, porque esto deja a nuestra Institución en un muy bajo nivel, ya que se ve desaseada como si no estuvieran estudiantes de una Institución Educativa, espero les guste nuestro vídeo.









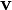 es constante; esto significa que no existe aceleración.
es constante; esto significa que no existe aceleración. en cualquier instante
en cualquier instante 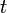 viene dada por
viene dada por .
.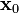 y un tiempo inicial
y un tiempo inicial 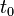 , ambos distintos de cero, la posición para cualquier tiempo está dada por
, ambos distintos de cero, la posición para cualquier tiempo está dada por






